众所周知,酗酒是一种不健康的生活方式,同时也是一个主要的可预防的死亡原因,酗酒会带来相当大的社会和经济负担。在这之中,青少年酗酒更是危险,青春期是大脑成熟的关键时期,在这一时期酗酒会增加未来患精神障碍疾病的风险。值得注意的是,杏仁核(amygdala)是产生、识别和调节情绪,以及控制学习和记忆的脑部组织,同时也是是调节酒精使用障碍(AUD)和焦虑障碍的关键大脑区域。在之前的研究中,研究团队已经发现,青少年酗酒会改变与早期基因活性调节相关的细胞骨架相关蛋白(Arc)的增强子区域的表观遗传修饰,并降低啮齿类动物和人类杏仁核中的 Arc 基因表达。Arc 可以对突触活动作出迅速而有力的反应,被认为是大脑可塑性的关键调节器。
众所周知,酗酒是一种不健康的生活方式,同时也是一个主要的可预防的死亡原因,酗酒会带来相当大的社会和经济负担。在这之中,青少年酗酒更是危险,青春期是大脑成熟的关键时期,在这一时期酗酒会增加未来患精神障碍疾病的风险。值得注意的是,杏仁核(amygdala)是产生、识别和调节情绪,以及控制学习和记忆的脑部组织,同时也是是调节酒精使用障碍(AUD)和焦虑障碍的关键大脑区域。在之前的研究中,研究团队已经发现,青少年酗酒会改变与早期基因活性调节相关的细胞骨架相关蛋白(Arc)的增强子区域的表观遗传修饰,并降低啮齿类动物和人类杏仁核中的 Arc 基因表达。Arc 可以对突触活动作出迅速而有力的反应,被认为是大脑可塑性的关键调节器。 大脑杏仁核由此看来,青少年酗酒导致的杏仁核 Arc 基因表观遗传重编程无疑与成年后的焦虑和酗酒倾向脱不开干系。在这项最新研究中,研究团队提出了通过基因编辑逆转这种表观遗传重编程的假设,并对其进行实验验证。该研究的通讯作者 Subhash Pandey 教授表示:“早期酗酒会对大脑产生持久而显著的影响,而这项研究结果证明,基因编辑是这些不良影响的潜在解药,可以帮助大脑恢复出厂设置,让那些青少年时期就开始酒精暴露的人重获新生!”
大脑杏仁核由此看来,青少年酗酒导致的杏仁核 Arc 基因表观遗传重编程无疑与成年后的焦虑和酗酒倾向脱不开干系。在这项最新研究中,研究团队提出了通过基因编辑逆转这种表观遗传重编程的假设,并对其进行实验验证。该研究的通讯作者 Subhash Pandey 教授表示:“早期酗酒会对大脑产生持久而显著的影响,而这项研究结果证明,基因编辑是这些不良影响的潜在解药,可以帮助大脑恢复出厂设置,让那些青少年时期就开始酒精暴露的人重获新生!”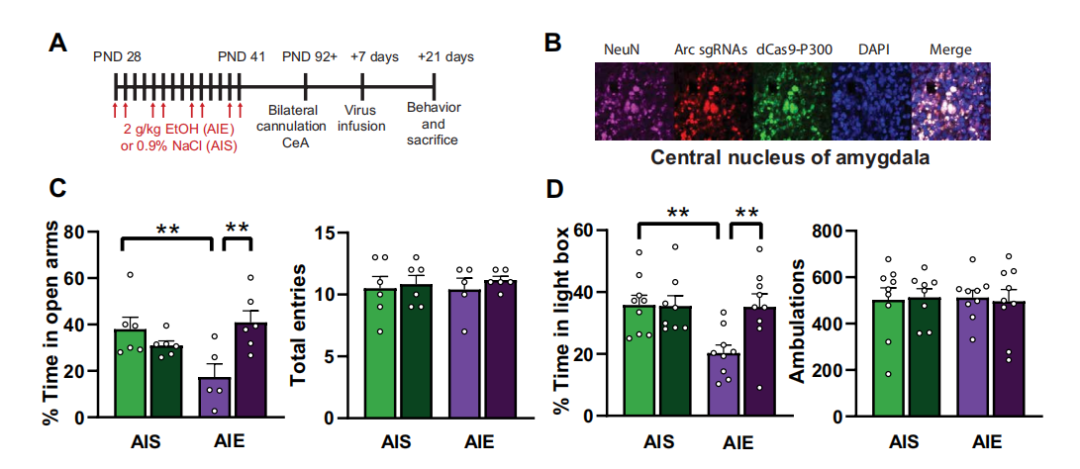 基因编辑逆转了青少年酒精暴露后在成年期的表观遗传学和行为后果研究团队对青春期间歇性饮酒的成年大鼠进行了研究,让这些大鼠在相对于人类10-18岁之间接触酒精。研究团队使用了 CRISPR-dCas9 的基因编辑调控工具,dCas9 因 DNA 双链切割活性丧失而不会切断 DNA 双链,但仍可以通过 gRNA 识别并结合到目标基因上。研究团队构建了 dCas9 和乙酰转移酶 P300 的融合蛋白,dCas9-P300 可以增加 Arc 的组蛋白乙酰化,并使酗酒导致的 Arc 表达缺陷正常化。不仅如此,研究团队还对这些大鼠进行了迷宫测试和酒精偏好测试。研究结果表明,经过 dCas9-P300 治疗的大鼠,其焦虑和饮酒的指标均有所下降。
基因编辑逆转了青少年酒精暴露后在成年期的表观遗传学和行为后果研究团队对青春期间歇性饮酒的成年大鼠进行了研究,让这些大鼠在相对于人类10-18岁之间接触酒精。研究团队使用了 CRISPR-dCas9 的基因编辑调控工具,dCas9 因 DNA 双链切割活性丧失而不会切断 DNA 双链,但仍可以通过 gRNA 识别并结合到目标基因上。研究团队构建了 dCas9 和乙酰转移酶 P300 的融合蛋白,dCas9-P300 可以增加 Arc 的组蛋白乙酰化,并使酗酒导致的 Arc 表达缺陷正常化。不仅如此,研究团队还对这些大鼠进行了迷宫测试和酒精偏好测试。研究结果表明,经过 dCas9-P300 治疗的大鼠,其焦虑和饮酒的指标均有所下降。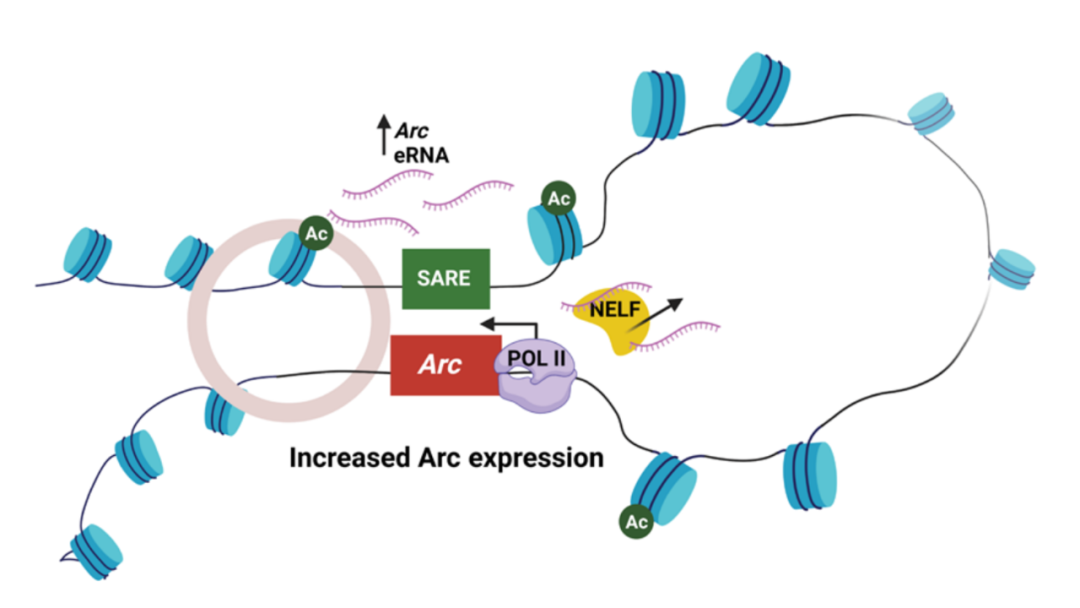 dCas9-P300可以增加Arc的组蛋白乙酰化,并使酗酒导致的Arc表达缺陷正常化研究小组还构建了 dCas9 和基因抑制元件 KRAB 的融合蛋白。即使是在没有早期酒精暴露的成年大鼠中,当使用 dCas9-KRAB 促进 Arc 基因的甲基化时,Arc 表达降低,这些大鼠的焦虑和饮酒指标也增加了。
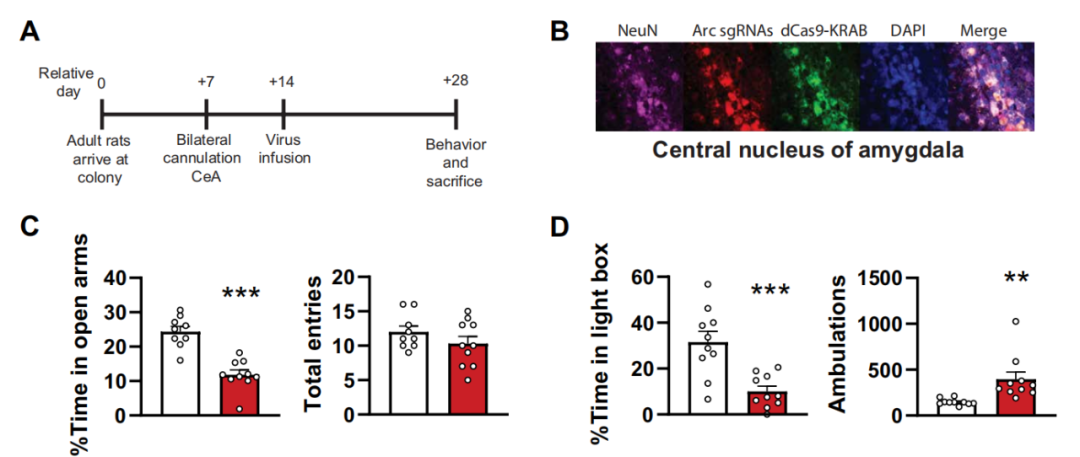
dCas9-P300可以增加Arc的组蛋白乙酰化,并使酗酒导致的Arc表达缺陷正常化研究小组还构建了 dCas9 和基因抑制元件 KRAB 的融合蛋白。即使是在没有早期酒精暴露的成年大鼠中,当使用 dCas9-KRAB 促进 Arc 基因的甲基化时,Arc 表达降低,这些大鼠的焦虑和饮酒指标也增加了。